Выше показано, что реакция чистой воды является нейтральной (рН = 7). Водные растворы кислот и оснований имеют, соответственно, кислую (рН < 7) и щелочную (рН > 7) реакцию. Практика, однако, показывает, что не только кислоты и основания, но и соли могут иметь щелочную или кислую реакцию - причиной этого является гидролиз солей. Взаимодействие солей с водой, в результате которого образуются кислота (или кислая соль), и основание (или основная соль), называется гидролизом солей. Рассмотрим гидролиз солей следующих основных типов: 1. Соли сильного основания и сильной кислоты (например, KBr, NаNО3) при растворении в воде не гидролизуются, и раствор соли имеет нейтральную реакцию….

Хорошо известно, что одни вещества в растворенном или расплавленном состоянии проводят электрический ток, другие в тех же условиях ток не проводят. Это можно наблюдать с помощью простого прибора. Он состоит из угольных стержней (электродов), присоединенных проводами к электрической сети. В цепь включена электрическая лампочка, которая показывает присутствие или отсутствие тока в цепи. Если опустить электроды в раствор сахара, то лампочка не загорается. Но она ярко загорится, если их опустить в раствор хлорида натрия. Вещества, распадающиеся на ионы в растворах или расплавах и потому проводящие электрический ток, называются электролитами. Вещества, которые в тех же условиях на ионы не распадаются и электрический ток не проводят, называются неэлектролитами. К электролитам относятся кислоты, основания и почти все соли, к неэлектролитам — большинство органических соединений,…
Для объяснения особенностей водных растворов электролитов шведским ученым С.Аррениусом в 1887 г. была предложена теория электролитической диссоциации. В дальнейшем она была развита многими учеными на основе учения о строении атомов и химической связи. Современное содержание этой теории можно свести к следующим трем положениям: 1. Электролиты при растворении в воде распадаются (диссоциируют) на ионы — положительные и отрицательные. Ионы находятся в более устойчивых электронных состояниях, чем атомы. Они могут состоять из одного атома — это простые ионы (Na+, Mg2+, Аl3+ и т.д.) — или из нескольких атомов — это сложные ионы (NО3—, SO2-4, РОЗ-4и т.д.). 2. Под действием электрического тока ионы приобретают направленное движение: положительно заряженные ионы движутся к катоду, отрицательно заряженные — к аноду. Поэтому первые называются катионами, вторые — анионами. Направленное движение ионов происходит в результате притяжения их противоположно заряженными электродами. 3. Диссоциация — обратимый процесс: параллельно с распадом молекул на ионы (диссоциация) протекает процесс соединения ионов (ассоциация). Поэтому в уравнениях электролитической диссоциации вместо знака равенства ставят знак обратимости. Например,…
![]()
Существенным является вопрос о механизме электролитической диссоциации. Легче всего диссоциируют вещества с ионной связью. Как известно, эти вещества состоят из ионов. При их растворении диполи воды ориентируются вокруг положительного и отрицательного ионов. Между ионами и диполями воды возникают силы взаимного притяжения. В результате связь между ионами ослабевает, происходит переход ионов из кристалла в раствор. При…
С помощью теории электролитической диссоциации дают определения и описывают свойства кислот, оснований и солей. Кислотами называются электролиты, при диссоциации которых в качестве катионов образуются только катионы водорода Н3РО4 Н+ + Н2РО—4(первая ступень) Н2РО—4 Н+ + НРO2-4 (вторая ступень) НРО2-4 Н+ PОЗ—4 (третья ступень) Диссоциация многоосновной кислоты протекает главным образом по первой ступени, в меньшей степени по второй и лишь в незначительной степени — по третьей. Поэтому в водном растворе, например, фосфорной кислоты наряду с молекулами Н3РО4 имеются ионы (в последовательно уменьшающихся количествах) Н2РО2-4, НРО2-4 и РО3-4. Основаниями называются электролиты, при диссоциации которых в качестве анионов образуются только гидроксид-ионы. Например: KOH K+ + OH—;…
Поскольку электролитическая диссоциация — процесс обратимый, то в растворах электролитов наряду с их ионами присутствуют и молекулы. Поэтому растворы электролитов характеризуются степенью диссоциации (обозначается греческой буквой альфа α). Степень диссоциации — это отношение числа распавшихся на ионы молекул N’ к общему числу растворенных молекул N: Степень диссоциации электролита определяется опытным путем и выражается в долях единицы или в процентах. Если α = 0, то диссоциация отсутствует, а если α = 1 или 100%, то электролит полностью распадается на ионы. Если же α = 20%, то это означает, что из 100 молекул данного электролита 20 распалось на ионы. Различные электролиты имеют различную степень диссоциации. Опыт показывает, что она зависит от концентрации электролита и от температуры. С уменьшением концентрации электролита,…
Согласно теории электролитической диссоциации все реакции в водных растворах электролитов являются реакциями между ионами. Они называются ионными реакциями, а уравнения этих реакций — ионными уравнениями. Они проще уравнений реакций, записанных в молекулярной форме, и имеют более общий характер. При составлении ионных уравнений реакций следует руководствоваться тем, что вещества малодиссоциированные, малорастворимые (выпадающие в осадок) и газообразные записываются в молекулярной форме. Знак ↓, стоящий при формуле вещества, обозначает, что это вещество уходит из сферы реакции в виде осадка, знак обозначает, что вещество удаляется из сферы реакции в виде газа. Сильные электролиты, как полностью диссоциированные, записывают в виде ионов. Сумма электрических зарядов левой части уравнения должна быть равна сумме электрических зарядов правой части. Для закрепления этих положений рассмотрим два примера. Пример 1. Напишите уравнения реакций между растворами хлорида железа (III) и гидроксида натрия в молекулярной и ионной формах. Разобьем решение задачи на четыре этапа. 1….
КH2O = 1.10-4 Данная константа для воды называется ионным произведением воды, которое зависит только от температуры. При диссоциации воды на каждый ион Н+ образуется один ион ОН—, следовательно, в чистой воде концентрации этих ионов одинаковы: [Н+] = [ОН—]. Используя значение ионного произведения воды, находим: = [ОН—] = моль/л. Таковы концентрации ионов Н+ и ОН—…
Существует 2 теории растворов : физическая и химическая .
Физическая теория растворов.
Была открыта Якобом Г. Вант-Гоффом и Свате А.Аррениусом.
Суть теории растворов : растворитель - химическая индифферентная среда, в которой равномерно распределены частицы растворенного вещества. Теория не предполагает наличие межмолекулярных связей между растворителем и растворенным веществом.
Под эту теорию подходят только идеальные растворы, где компоненты растворителя никак не воздействуют на растворимое соединение. Примером являются газовые растворы, где нереагирующие между собой газы смешиваются друг с другом в неограниченных количествах. Все физические данные (температура кипения и плавления, давление, теплоемкость) вычисляется исходя из свойств всех соединений, входящих в состав.
По закону Дальтона : общее давление газовой смеси равно сумме парциальных давлений ее компонентов:
P общ = Р 1 + Р 2 + Р 3 +…
Химическая теория растворов.
Химическую (сольватную) теорию растворов описал Д.И. Менделеев . Суть заключается в следующем: частицы растворителя и растворенного вещества реагируют друг с другом, в результате чего получаются нестойкие соединения переменного состава - гидраты (сольваты ). Основные связи тут - водородные.
Вещество может распадаться на слои (растворяться) в случае полярного растворителя (воды). Ярким примером является растворение поваренной соли.
Также может проткать реакция между компонентами смеси:
H 2 O +Cl 2 = HCl + HOCl ,
В ходе процесса растворения происходит изменение состава и объема реакционной смеси, т.к. протекают 2 процесса: разрушение структуры растворяемого вещества и химическая реакция между частицами. Оба процесса идут с изменением энергии.
Тепловые эффекты могут быть экзотермическими и эндотермическими (с выделением и поглощением энергии).
Соединения с частицами растворителя называются гидратами .
Кристаллические вещества, в состав которых входят гидраты, называются кристаллогидратами и имеют различную окраску. Например, кристаллогидрат сульфата меди: CuSO 4 ·5 H 2 О . Раствор кристаллогидрата синий. Если рассмотреть кристаллогидрат кобальта CoCl 2 · 6 H 2 O , то он обладает розовым цветом, CoCl 2 · 4 H 2 O - красный, CoCl 2 ·2 H 2 O - сине-фиолетовый, CoCl 2 · H 2 О - темно-синий, а безводный раствор хлорида кобальта - бледно-синего цвета.


конце XIX века растворы считались физическими образованиями, в которых отсутствуют какие-либо взаимодействия между растворителем и растворенным веществом. Образование раствора объяснялось диспергированием частиц растворенного вещества в индифферентной среде растворителя. Основоположниками этих взглядов были такие известные ученые, как Я. Вант-Гофф, С. Арре-ниус и В. Оствальд. В 1887 году великий русский химик Д. И. Менделеев, опираясь на многочисленные экспериментальные данные, создал химическую (гидратную) теорию растворов. Основой этой теории была идея о химическом характере растворения. В растворе образуются соединения между растворенным веществом и растворителем, изменяющие свой состав с изменением температуры и концентрации. Эти соединения были названы Д. И. Менделеевым гидратами, или - сольватами. Образующиеся гидраты имеют различную прочность. Большинство из них неустойчиво и существует только в растворах. Однако некоторая часть гидратов является настолько прочными соединениями, что при выделении растворенного вещества из раствора вода входит в состав растущего кристалла в химически связанном виде. Такие кристаллы были названы кристаллогидратами, а входящая в их состав вода - кристаллизационной. Примерами кристаллогидратов являются CuS04 5Н20; Na2S04 ЮН20 и др. Прочность образующихся соединений определяется силами, действующими между растворителем и растворенным веществом. В настоящее время известна природа этих сил. СольватЫ (гидраты) образуются за счет ион-дипольного, диполь-ди-польного, донорно-акцепторного взаимодействия, за счет водородных связей, а также дисперсионного взаимодействия. Менделеев не отрицал роль физического фактора при образовании растворов. Он писал: «Две указанные стороны растворения (физическая и химическая) и гипотезы, до сих пор приложенные к рассмотрению растворов, хотя имеют отчасти различные исходные точки, со временем приведут к общей теории растворов, потому что одни общие законы управляют как физическими, так и химическими явлениями». Взгляды Д. И. Менделеева полностью подтвердились. В настоящее время процесс растворения рассматривают как физико-химический процесс, а растворы - как физико-химические системы. Химическая теория растворов Д. И. Менделеева позволяла объяснить наличие тепловых эффектов, возникающих при процессах растворения веществ. Тепловой эффект процесса растворения (ДНраств) можно представить в виде суммы теплоты, необходимой для разрушения кристаллической решетки вещества (ДНре1:1) и теплоты, выделяющейся в процессе сольватации (ДНсольват), т. е. AHp^ является значительной эндотермической величиной, а ДНС0ЛЬВ близкая к ней по значению экзотермическая величина. Исходя из этого, конечный знак теплового эффекта процесса растворения будет определяться величиной вклада каждого из этих параметров. При растворения эндотермичен. Это можно наблюдать, например, при растворении в воде нитратов калия и аммония, хлорида калия и др. При процесс растворения экзотермичен. Примером этого является растворение в воде хлоридов кальция и магния, гидроксидов натрия и калия и др. Итак, знак теплового эффекта определяется природой растворенного вещества и растворителя, глубиной их взаимодействия между собой. Наличием химического взаимодействия между компонентами объясняются и объемные эффекты при растворении. Так, при растворении 1 л этилового спирта в 1 л воды объем образующегося раствора оказывается равным не 2 л, а 1,93 л. В этом случае уменьшение объема обусловлено, в основном, образованием водородных связей между гидроксильными группами воды и спирта.
В середине XIX века общепринятой считалась физическая теория растворов, одним из авторов которой являлся Вант-Гофф (Голландия). Эта теория рассматривала растворы как механические смеси, без учета взаимодействий между молекулами растворителя и частицами растворенного вещества.
Факты, которые не могла объяснить физическая теория растворов:
1) Тепловые эффекты растворения.
Пример. Растворение – процесс экзотермический; растворение – эндотермический.
2) Изменение (чаще – уменьшение) объема жидкости при растворении. Это явление называется контракция.
Пример. При смешивании 50 мл и 50 мл образуется 98 мл раствора
3) Изменение окраски некоторых веществ при растворении и некоторых растворов при выпаривании.
Примеры. Безводный сульфат меди(II) – белый порошок – при поглощении воды синеет.
Розовый раствор хлорида кобальта(II) при высыхании окраску не изменяет, а при последующем выпаривании – синеет.
1),2),3) - признаки химических реакций.
Д. И. Менделеев считал, что рассмотренные явления, безусловно, указывают на какие-то взаимодействия между растворенным веществом и растворителем. Он последовательно развивал мысль о химическом взаимодействии между частицами растворенного вещества и молекулами растворителя. Учение Менделеева было развито и дополнено русскими учеными И. А. Каблуковым и В. А. Кистяковским. На основе этих представлений произошло объединение физической и химической точки зрения на растворы.
Основные положения современной физико-химической теории растворов сводятся к следующему.
1) Растворитель и растворенное вещество химически взаимодействуют между собой.
2) В результате взаимодействия образуются непрочные соединения, называемые сольватами, а сам процесс называется сольватацией. В частном случае, когда растворителем является вода, эти соединения называются гидратами, а процесс – гидратацией.
Сами растворы, а также большинство гидратов (сольватов), которые образуются при растворении, имеют переменный состав. Этим они отличаются от химических соединений.
Физико-химическая теория растворов позволила объяснить многие непонятные до этого факты:
1) Изменение окраски некоторых веществ при растворении и некоторых растворов при выпаривании.
2) Тепловые эффекты при растворении.
Явление гидратации иногда можно наблюдать, не пользуясь специальными приборами. Например, безводный сульфат меди (II) CuSO 4 – белое вещество. При его растворении в воде образуется голубой раствор. Окраска раствора обусловливается гидратированными ионами меди. Гидратированные частички иногда настолько прочны, что при выделении растворенного вещества из раствора в твердую фазу молекулы воды входят в состав кристаллов. Так, при выпаривании водного раствора сульфата меди в твердую фазу выделяется соль CuSO 4 ∙5H 2 O.
Кристаллические вещества, в состав которых входят молекулы воды, называются кристаллогидратами, а содержащаяся в них вода - кристаллизационной
Аналогично объясняется изменение окраски раствора хлорида кобальта(II) при выпаривании. Гидратированные ионы кобальта в растворе - розового цвета, такой же розовый цвет имеет и кристаллогидрат кобальта (II) CoCl 2 ∙6H 2 O. Но при прокаливании на воздухе кристаллогидрат кобальта теряет кристаллизационную воду и превращается в безводный хлорид кобальта(II) синего цвета.
Образованием кристаллогидратов объясняются и тепловые эффекты при растворении. Тепловой эффект растворения складывается из энергии, затраченной на разрушение кристаллической решетки и отделение частиц растворенного вещества друг от друга, а также энергии, которая выделяется при гидратации.
Какой вклад энергии преобладает, такой тепловой эффект в итоге мы и получаем.
Изменение других термодинамических параметров при растворении.
Так как, в целом, при растворении беспорядок в системе увеличивается.
Так как растворение – процесс самопроизвольный.
Химическая, или сольватная, теория растворов была предложена в 1887 г. Д.И. Менделеевым, который установил, что в реальном растворе присутствуют не только индивидуальные компоненты, но и продукты их взаимодействия. Исследования водных растворов серной кислоты и этилового спирта, проведенные Д.И. Менделеевым, легли в основу теории, суть которой заключается в том, что между частицами растворенного вещества и молекулами растворителя происходят взаимодействия, в результате которых образуются нестойкие соединения переменного состава, называемые сольватами или гидратами , если растворителем является вода. Главную роль в образовании сольватов играют непрочные межмолекулярные силы, в частности, водородная связь.
В этой связи следует принять следующую трактовку понятия «раствор»:
Раствором называется гомогенная система переменного состава, состоящая из двух и более компонентов и продуктов их взаимодействия.
Из данного определения следует, что растворы занимают промежуточное положение между химическими соединениями и смесями. С одной стороны, растворы однородны, что позволяет рассматривать их как химические соединения. С другой стороны, в растворах нет строгого стехиометрического соотношения между компонентами. Кроме того, растворы можно разделить на составные части (например, при упаривании раствора NaCl можно выделить соль в индивидуальном виде).
Основные способы выражения концентрации растворов
Количественный состав раствора чаще всего оценивают при помощи понятия концентрации , под которым понимают содержание растворенного вещества (в определенных единицах) в единице массы (объема) раствора (растворителя). Основными способами выражения концентрации растворов являются следующие:
1. Массовая доля вещества (x ) это отношение массы данного компонента x, содержащегося в системе, к общей массе этой системы:
Единицей количества вещества является моль, т. е. то количество вещества, которое содержит столько реальных или условных частиц, сколько атомов содержится в 0,012 кг изотопа С 12 . При использовании моля как единицы количества вещества следует знать, какие частицы имеются в виду: молекулы, атомы, электроны или другие. Молярная масса М(х) это отношение массы к количеству вещества (г/моль):
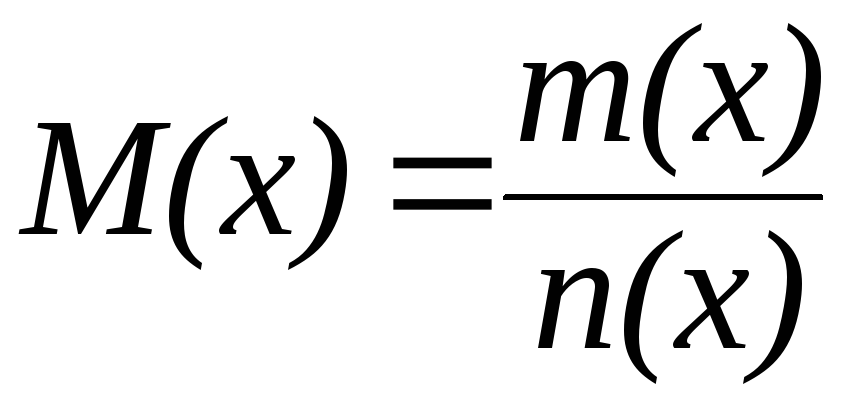
3. Молярная концентрация эквивалента С(x ) это отношение количества эквивалента вещества n(x) к объему раствора V р-ра:
|
|
Химический эквивалент – это реальная или условная частица вещества, которая может замещать, присоединять или высвобождать 1 ион водорода в кислотно-основных или ионообменных реакциях.
Так же, как молекула, атом или ион, эквивалент безразмерен.
Масса моля эквивалентов называется молярной массой эквивалента М(x ). Величина называется фактором эквивалентности . Она показывает, какая доля реальной частицы вещества соответствует эквиваленту. Для правильного определения эквивалента вещества надо исходить из конкретной реакции, в которой это вещество участвует, например, в реакции взаимодействия Н 3 РО 4 с NaOH может происходить замещение одного, двух или трех протонов:
1. H 3 PO 4 + NaOH NaH 2 PO 4 + H 2 O;
2. H 3 PO 4 + 2NaOH Na 2 HPO 4 + 2H 2 O;
3. H 3 PO 4 + 3NaOH Na 3 PO 4 + 3H 2 O.
В
соответствии с определением эквивалента,
в 1-й реакции замещается один протон,
следовательно, молярная масса эквивалента
вещества равна молярной массе, т. е.
z l
и 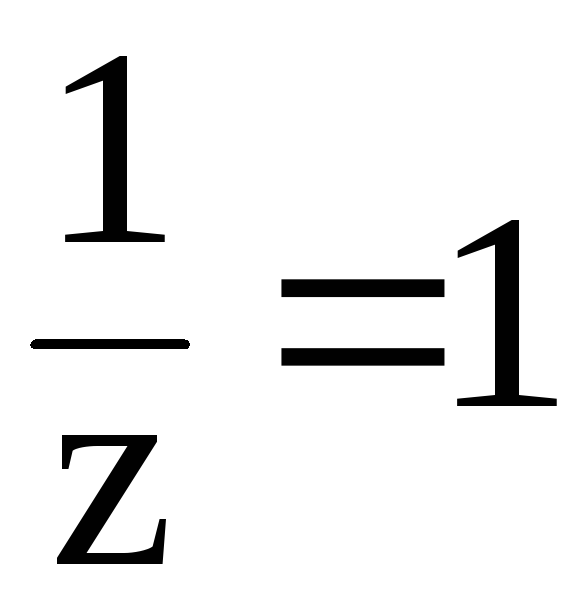 .
В данном случае:
.
В данном случае:
Во 2-й
реакции происходит замещение двух
протонов, следовательно, молярная масса
эквивалента составит половину молярной
массы Н 3 РО 4 ,
т. e.
z 2,
а .
Здесь:
.
Здесь:
В 3-й реакции
происходит замещение трех протонов и
молярная масса эквивалента составит
третью часть молярной массы Н 3 РО 4 ,
т.е. z 3,
a
 .
Соответственно:
.
Соответственно:
В реакциях обмена, где непосредственно не участвуют протоны, эквиваленты могут быть определены косвенным путем, введением вспомогательных реакций, анализ результатов которых позволяет вывести правило, что z для всех реакций равен суммарному заряду обменивающихся ионов в молекуле вещества, участвующего в конкретной химической реакции.
1. AlCl 3 + 3AgNO 3 = Al(NO 3) 3 + 3AgCl.
Для AlCl 3 обменивается 1 ион Al 3+ с зарядом +3, следовательно, z = 13 = 3. Таким образом:
Можно также сказать,
что обмениваются 3 иона хлора с зарядом
1.
Тогда z = 31 = 3
и

Для AgNO 3 z = 11 = 1 (обменивается 1 ион Ag + с зарядом +1 или обменивается 1 ион NO 3 с зарядом 1).
2. Al 2 (SO 4) 3 + 3BaCl 2 = 3BaSO 4 + 2AlCl 3 .
Для Al 2 (SO 4) 3 z = 23 = 6 (обменивается 2 иона Al 3+ с зарядом +3 или 3 иона SO 4 2 с зарядом 2). Следовательно,
Итак,
запись С(H 2 SO 4)
= 0,02 моль/л означает, что имеется раствор,
в 1 л которого содержится 0,02 моль
эквивалента H 2 SO 4 ,
а молярная масса эквивалента H 2 SO 4
составляет при этом
молярной массыH 2 SO 4 ,
т. е. 1 л раствора содержит
 H 2 SO 4 .
H 2 SO 4 .
При
факторе эквивалентности  молярная концентрация эквивалента
равна молярной концентрации раствора.
молярная концентрация эквивалента
равна молярной концентрации раствора.
4. Титр Т(x ) – это отношение массы вещества к объему раствора (в мл):
6. Мольная доля N(x ) – это отношение количества вещества данного компонента,содержащегося всистеме, к общему количеству веществ системы:
|
|
Выражается в долях единицы или в %.
7. Коэффициентом растворимости вещества Р(x ) называют максимальную массу вещества, выраженную в г, которая может раствориться в 100 г растворителя.


